湖南师范大学何祖平教授团队最近研究发现,OIP5通过与NCK2蛋白相互作用调节人精原干细胞的自我更新、DNA合成和凋亡等生物学过程,且OIP5的异常表达或突变可能与非梗阻性无精子症(NOA)的发生相关。相关成果以“OIP5 Interacts with NCK2 to Mediate Human Spermatogonial Stem Cell Self-Renewal and Apoptosis through Cell Cyclins and Cycle Progression and Its Abnormality Is Correlated with Male Infertility”为题发表在Research上。
Citation:
Cui Y,Chen W,Du L,He Z. OIP5 Interacts with NCK2 to Mediate Human Spermatogonial Stem Cell Self-Renewal and Apoptosis through Cell Cyclins and Cycle Progression and Its Abnormality Is Correlated with Male Infertility. Research. 2023:6;0162. DOI: 10.34133/research.0162.
研究背景
精子发生是指精原干细胞(Spermatogonial stem cells,SSCs)自我更新与分化为精子的复杂过程。精原干细胞作为睾丸中的成体干细胞,是持续精子发生和维持男性生育力的基础。解析精原干细胞生物学功能的分子调控机理对于理解男性不育症的发病机制与诊治具有重要意义。
OIP5仅在部分肿瘤细胞和睾丸中特异表达,被定义为肿瘤-睾丸特异性基因。其编码一个25 kDa带有卷曲螺旋结构域的蛋白,对细胞周期调控有至关重要的作用。研究表明,OIP5在调节肿瘤细胞增殖、凋亡及周期等生物学过程具有重要作用。但OIP5在生殖系统中的作用及其调控机理尚不清楚。
研究进展
作者团队前期研究表明,PAK1可通过PDK1/KDR/ZNF367和ERK1/2和AKT途径促进人精原干细胞系的增殖并抑制其凋亡。通过RNA测序发现,PAK1敲低后导致人精原干细胞系OIP5基因水平降低,提示OIP5调控人精原干细胞的自我更新功能。首先,作者对OIP5在睾丸组织中的表达和定位进行探索,发现OIP5在睾丸中精原细胞和精母细胞中高表达(图1)。
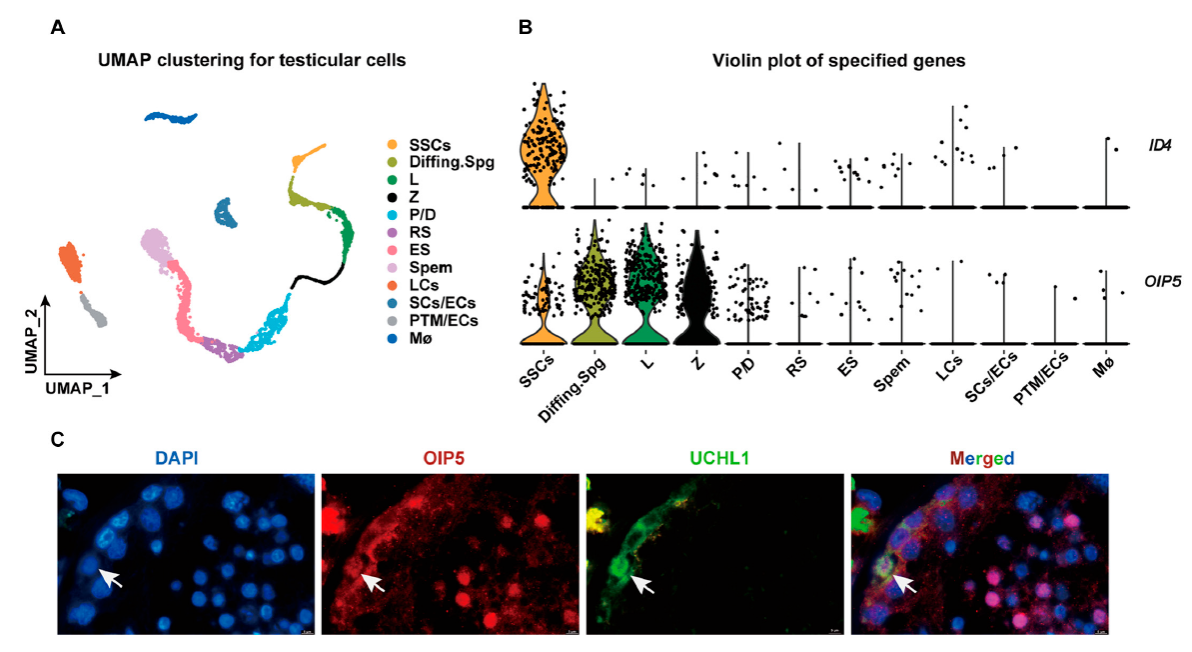
图1.OIP5在睾丸中的表达和定位
作者利用前期构建的人精原干细胞系和精原干细胞移植分别从体内外水平论证了OIP5沉默抑制人精原细胞系增殖与DNA合成,增加细胞凋亡,抑制细胞周期相关蛋白表达及细胞周期进程(图2)。
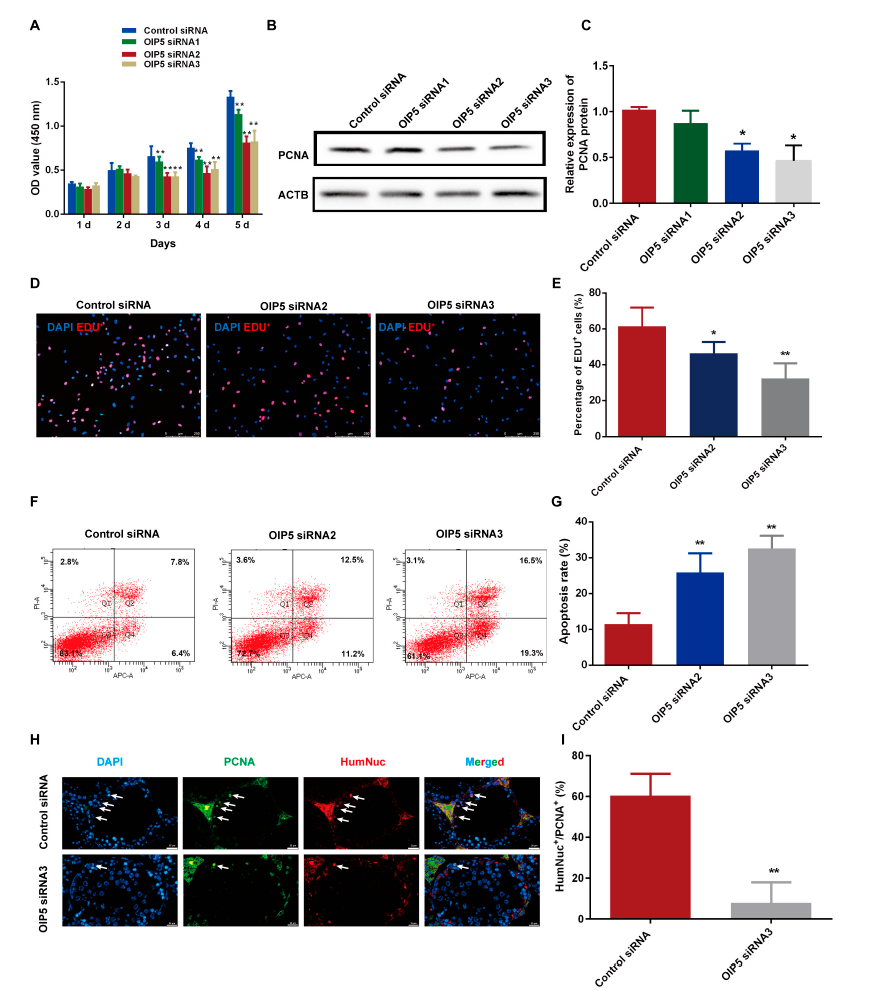
图2.OIP5沉默抑制人精原干细胞的生物学功能
RNA深度测序发现,OIP5敲低后NCK2和CCND1等基因显著下调。利用免疫沉淀和质谱(IP-MS)寻找OIP5的相互作用蛋白,并通过Co-IP和GST-Pulldown验证,揭示OIP5与NCK2存在相互作用(图3),且OIP5沉默降低NCK2的表达水平。
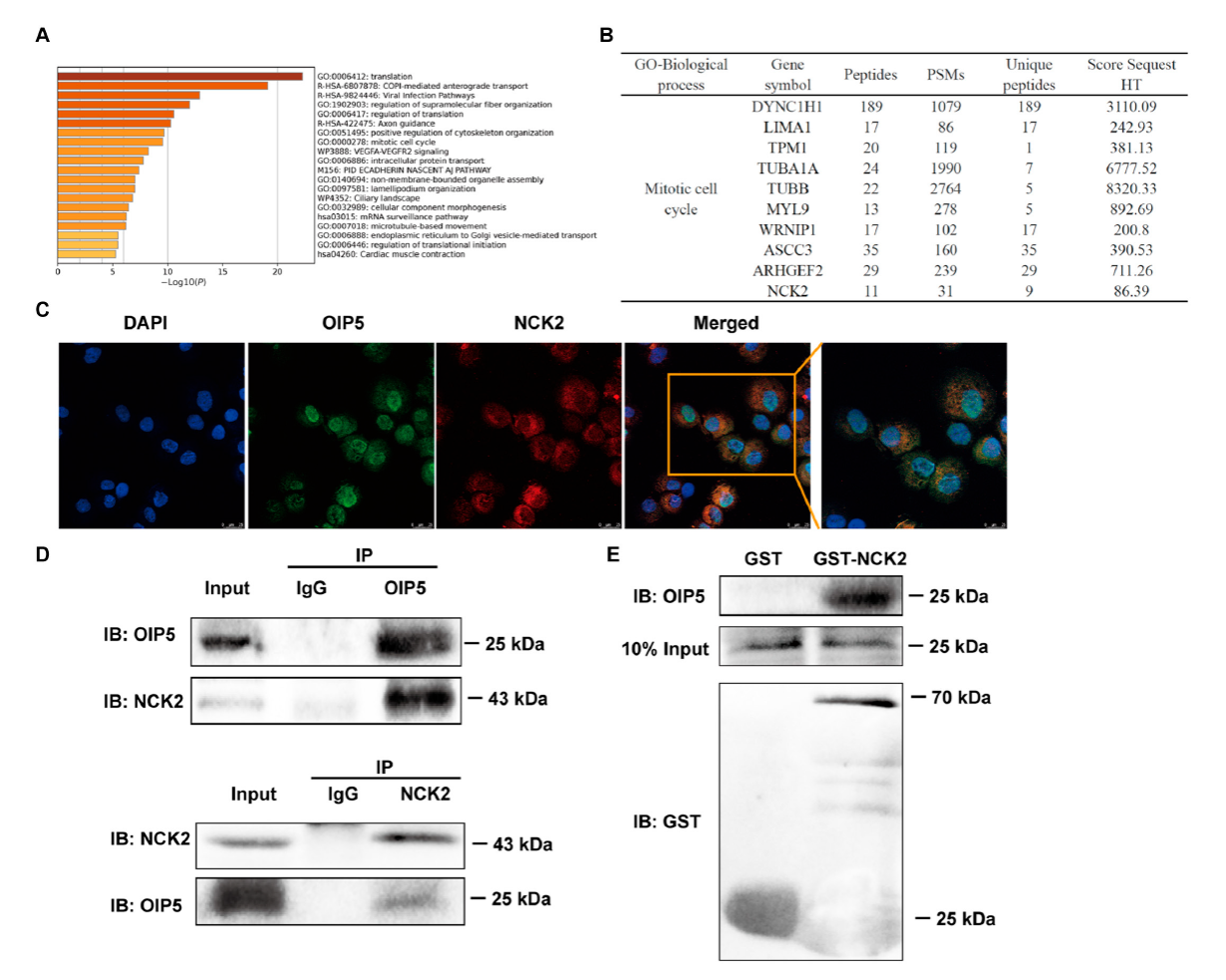
图3.OIP5与NCK2在人精原干细胞存在相互作用
NCK2是受体蛋白酪氨酸激酶的辅因子,含有三个SH3结构域和一个SH2结构域,在全身广泛表达。作者发现,NCK2敲低抑制人精原细胞系增殖与DNA合成,并促进其凋亡(图4)。
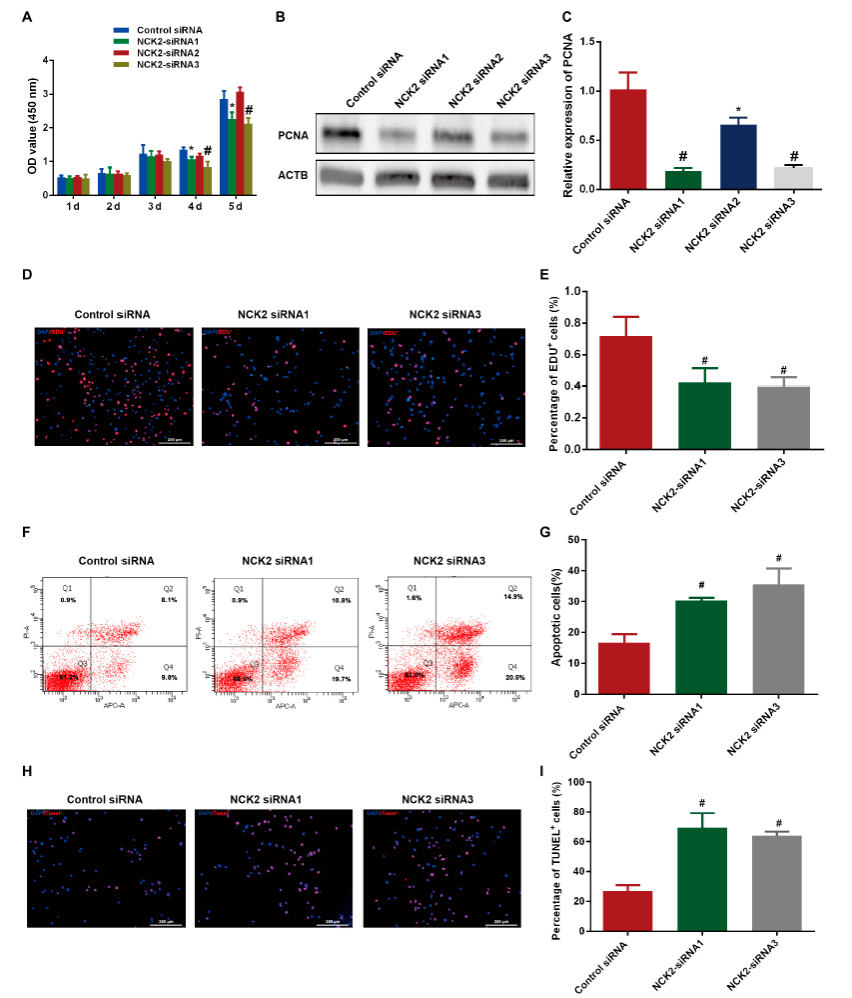
图4.NCK2沉默抑制人精原干细胞的生物学功能
有趣的是,作者对777个男性生精障碍的患者中进行了全外显子测序和测序结果分析及筛选,发现54例OIP5基因SNP突变(6.95%),包括1例纯合突变(c.494 C>T,p.S165F)及53例杂合突变。通过在线软件PolyPhen-2、GenoCanyon及ClinPred等筛选OIP5具有潜在危害性的变异;采用SPSS24.0对OIP5基因型频率进行卡方检验,对存在统计学差异的位点再进行logistic回归分析,阐明变异位点与NOA患病的相关性,发现rs560529830位点变异与NOA的患病风险呈正相关,提示OIP5可能与男性生精障碍相关(图5)。接下来,作者收集了不同病理类型的非梗阻性无精子症患者睾丸组织,发现OIP5在精母细胞阻滞和精原细胞阻滞患者睾丸中低水平表达(图5)。
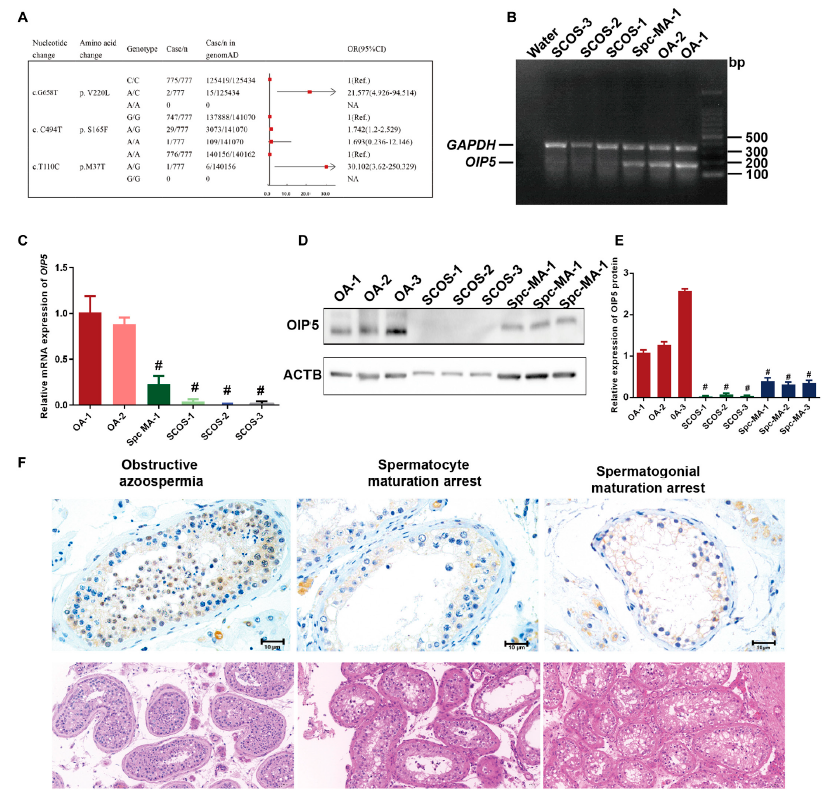
图5.OIP5突变与低表达水平与非梗阻性无精子症的相关性
未来展望
OIP5是一个高度保守的蛋白,有可能作为精子发生障碍的标记物或治疗靶点。在本研究中,作者首次论证了OIP5对人精原干细胞自我更新与凋亡的重要调控作用,并且发现OIP5突变或低表达水平可能与非梗阻性无精子症的发生相关性。该研究为理解男性不育症的发病机制及其诊治提供新的分子机理与靶标。
通讯作者简介
何祖平博士,二级教授,博士生导师,湖南师范大学医学院院长,“潇湘学者”特聘教授,上海高校特聘教授(东方学者),湖湘高层次人才聚焦工程-杰出创新人才,“模式动物与干细胞生物学”湖南省重点实验室主任、“生殖与转化医学”湖南省工程研究中心主任。主持国家自然科学基金重点项目、国家重点研发计划课题、国家重大科学研究课题(2项)、国家自然科学基金面上项目(4项)、湖南省重大专项课题、湖南省重点研发计划项目、上海市科委重点项目、湖南省教育厅重点项目。“临床医学”国家一流专业建设点负责人,“基础医学”湖南省“十四五”重点学科建设负责人。他长期从事生殖医学、细胞生物学与分子生物学研究。其研究成果以通讯作者发表在国际著名期刊,如Cell Death and Differentiation、Cell Death and Disease等。他以通讯作者或第一作者已发表或接受发表SCI收录论文83篇,合计SCI影响因子(IF)>390;IF>5论文40篇,论文被Nature Genetics、Cell Stem Cell等SCI引用2800多次。单篇论文最高SCI引用次数291次。担任SCI期刊Frontiers in Cell and Developmental Biology副主编、Asian Journal of Andrology编委、Innovation副主编、湖南师范大学学报(医学版)主编。获得湖南省自然科学奖二等奖、教育部科技进步奖二等奖、上海市医学科技一等奖。
编辑:刘凯轩
责编:朱天爱
审核:鄢朝晖